|
医疗器械警戒快讯 2026年第4期(总第230期)
发布日期:2026-05-13
医疗器械警戒快讯
(总第230期)
内容提要
美国FDA发布关于Arrow International公司召回包含Merit Medical公司可撕开导管鞘的透析导管套件的警示信息 发布日期:2026年4月24日 CDRH发布早期警示信息以提醒公众关注潜在高风险医疗器械问题。FDA将持续向公众通报新的重要信息并在网页更新相关内容。 受影响的产品 FDA注意到,Arrow International公司已致信受影响的客户,建议将含有Merit Medical公司生产的16F双阀可撕开导管鞘的透析导管套件从使用或销售的地方移除。
完整受影响产品清单请见网页: https://www.fda.gov/medical-devices/medical-device-recalls-and-early-alerts/early-alert-arrow-international-removes-dialysis-catheter-kits-containing-merit-medical-splittable 产品用途 16F双阀可撕开导管鞘是Arrow几个血液透析导管套件中使用的组件,成品采用无菌包装。可撕开导管鞘用于将导管送入血管系统。 警示原因 Arrow International公司针对包含受Merit Medical公司透析导管召回信息影响产品的透析导管套件发起了紧急医疗器械召回通知。 Merit Medical公司正在召回16F双阀可撕开导管鞘,原因是设计缺陷,导管鞘可能无法按预期拆分。这种导管鞘用于几种受影响的Arrow透析导管套件。可撕开导管鞘未能按预期劈开可能导致出血、异物、手术延迟、栓塞/血栓形成、导管功能受损、未来血管通路的血管丧失。 截至2月23日,Merit Medical公司报告了与此问题有关的2例严重伤害事件,没有死亡事件。截至4月21日,Arrow International公司没有报告任何其他的患者伤害或死亡。 采取措施 不要使用Arrow International公司透析导管套件中包含的Merit Medical公司生产的16F双阀可撕开导管鞘。 2026年4月,Arrow International公司向所有受影响的客户发出了一封信,建议采取以下行动:
查看FDA相关网页信息了解最新情况。FDA目前正在审查有关这一潜在高风险产品问题的信息,并将在获得重要新信息时向公众通报。 (美国FDA网站)
美国FDA发布关于Aligned Medical Solutions公司手术器械便利组合包的早期警示信息 发布日期:2026年4月23日 CDRH发布早期警示信息以提醒公众关注潜在高风险医疗器械问题。FDA将持续向公众通报新的重要信息并在网页更新相关内容。 受影响的产品 FDA获悉,Aligned Medical Solutions(AMS)公司已向受影响的客户发出信函,建议将手术器械便利组合包中的某些血管造影注射器从使用或销售地方移除。 受影响组件包括: Medline注射器:10ml带旋转接头的血管注射器 Medline部件号:80085007 AMS注射器:10cc聚碳酸酯控制注射器(带旋转接头) AMS部件号:39331 批号:70209、71257、72311、75764、77812、80915、86214、94136、102993、108049、123896、127096、135426、140436、189197 受影响组合包:
产品用途 便利组合包中包含多种手术器械,敷料和/或其他材料,以及药物成分,这些器械旨在用于各种外科手术。 警示原因 Aligned Medical Solutions公司针对包含受Medline公司带旋转接头的Namic血管造影控制注射器(“Namic RA注射器”)召回信息影响产品的器械便利组合包,发出了紧急医疗器械召回通知。 Medline Industries公司表示,受影响产品上注射器旋转接头在使用过程中可能会松脱,导致注射器与歧管之间的连接松动或完全断开。如果发生松脱,则可能存在生物危害暴露、失血和感染的风险。连接松动或断开可能会使空气进入管路,从而可能导致空气栓塞。这些情况都可能导致严重伤害或死亡。所有器械都有可能出现这种故障模式。 截至3月13日,Medline Industries公司已报告4份与此问题相关的严重伤害事件,无死亡事件。 采取措施 识别装有受影响注射器的器械便利组合包。将附加标签贴在所有受影响的组合包上,说明必须移除并丢弃受影响的注射器,不得继续使用。 4月1日,Aligned Medical Solutions公司向所有受影响的客户发送了一封信函,建议他们采取以下行动:
查看FDA相关网页信息了解最新情况。FDA目前正在审查有关这一潜在高风险产品问题的信息,并将在获得重要新信息时向公众通报。
美国FDA发布关于Integra LifeSciences公司因拆卸风险召回颅骨钻适用Codman一次性钻头的风险警示信息 发布日期:2026年4月23日 召回级别:FDA已经确认此次召回为最严重的等级,如果继续使用此产品,可能会导致严重伤害或死亡。此次召回涉及从使用单位或销售机构撤回相关产品。 受影响的产品
查看受影响产品的完整信息请登录网址:https://products.integralife.com/file/general/14mm_codman_disposable_perforator_disassembly_recall_list_of_impacted_lots.pdf 产品用途 Codman一次性钻头是在神经外科手术中使用的一次性手术工具,用于在颅骨上钻孔,在钻孔完成后自动脱离。 召回原因 Integra LifeSciences公司正在召回特定的Codman一次性钻头和开颅手术工具包,原因是该产品保护套上的超声焊接不充分。这种焊接缺陷可能导致使用钻头进行开颅手术时,在使用之前、期间或之后解体。在某些情况下,钻头可能无法分离,从而阻止钻头立即停止。 使用受影响的产品可能会导致严重的不良健康后果,包括硬脑膜损伤、出血、脑损伤、长期手术、不可逆脑损伤和死亡。 已收到10份伤害报告,包括手术延迟、钻头在使用过程中卡在患者颅骨内、取出产品碎片困难、出血、硬脑膜损伤和脑损伤。还没有导致死亡的相关报告。 采取措施 2025年4月11日,Integra LifeSciences公司向所有受影响的客户发送了紧急医疗器械召回通知。2025年9月26日,Integra公司发出了第二份扩大召回范围的通讯。这些函件建议采取以下行动: (美国FDA网站)
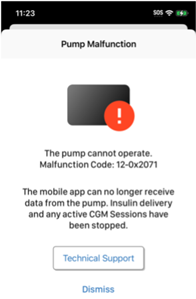
美国FDA发布关于Tandem Diabetes Care公司Tandem Mobi胰岛素泵的警示信息 发布日期:2024年4月22日 召回级别:本次召回涉及对产品进行纠正,不涉及将其从使用单位或销售机构移除。FDA已经确认此次召回为最严重的等级。如果在未进行纠正的情况下继续使用该产品,可能会导致严重伤害或死亡。 受影响的产品 FDA获悉,Tandem Diabetes Care公司已向受影响客户发布了一封紧急医疗器械纠正函,建议在继续使用前对所有软件版本为7.6.0.1、7.6.0.3和7.7.0.1的Tandem Mobi胰岛素泵进行纠正。
产品用途 Tandem胰岛素泵是电池驱动的输液泵,能够同时进行基础量和餐前大剂量胰岛素输送。该胰岛素泵利用电机驱动,从一次性药筒中通过输注管路将胰岛素输送至患者的皮下组织。 更正原因 Tandem Diabetes Care公司表示,运行受影响软件版本的Tandem Mobi胰岛素泵可能会错误地检测到电机问题,即所谓的假性电机故障。 除声音通知外,Mobi胰岛素泵内置振动电机,可为任何警报、警告或故障提供触觉反馈。在正常使用期间,Mobi胰岛素泵软件会监控使用过程中流经振动电机的电流。如果在胰岛素泵的定期监控期间检测到振动电机电流超出范围,将触发泵故障并通知用户(故障12)。如果胰岛素泵错误地
检测到电机问题,可能会导致胰岛素泵触发故障12。如果您的Tandem Mobi胰岛素泵显示故障12,胰岛素输送将停止,泵将无法操作。 故障12发生时,胰岛素将停止输送,并终止胰岛素泵与连续血糖监测(CGM)设备以及Tandem Mobi移动应用程序之间的通信。如果不及时处理,可能导致高血糖,因为功能故障会停止胰岛素输送,并导致实时连续血糖监测(CGM)估计葡萄糖值(EGVs)和CGM趋势中断。在严重高血糖情况下,用户可能需要住院或接受医疗专业人员的干预。 截至2025年11月4日,Tandem Diabetes Care公司已报告4起严重伤害事件,未发生与该问题相关的死亡案例。 采取措施 尽快更新您的胰岛素泵软件。准备好备用的胰岛素输送方法。 2025年10月6日,Tandem Diabetes Care公司向所有受影响的客户发送了紧急医疗器械更正通知,建议采取以下措施:
(美国FDA网站)
美国FDA发布关于Stryker公司对患者定制TMJ植入物 更新使用说明的警示信息 发布日期:2026年4月15日 召回级别:本次召回涉及对使用单位或销售机构的相关产品进行校正。FDA已经确认此次召回为最严重的等级。如果在未进行校正的情况下继续使用该产品,可能会导致严重伤害或死亡。 受影响的产品: FDA获悉,Stryker公司已向受影响的客户发出通知,提示某些TMJ单侧和双侧植入物已经更新了使用说明。 受影响产品完整列表详见FDA网站: https://www.fda.gov/medical-devices/medical-device-recalls-and-early-alerts/reconstruction-prosthesis-correction-stryker-updates-use-instructions-patient-fitted-tmj-implants 产品用途 TMJ Concepts患者定制颞下颌关节重建假体系统旨在用于颞下颌关节的重建。 更正原因 Stryker公司表示,他们收到1份报告称,在植入该产品的手术过程中,一颗6毫米长的螺钉被植入约2.6毫米厚的骨骼中,并穿透了颅顶。 设计规格表中指定的螺钉孔位置与实际颅窝结构之间存在差异。当植入物的螺钉孔位于骨质较薄区域时,可能导致推荐的螺钉长度超过骨厚度,从而穿透颅骨。颅骨穿透可能导致硬膜组织损伤、出血、脑脊液(CSF)漏出或脑膜炎。若使用受影响的产品,可能需要采取干预措施以防止严重伤害。 截至2025年12月4日,Stryker公司报告了1份与此问题相关的严重伤害事件,没有相关的死亡报告。 采取措施 继续按照您的随访方案对植入上述产品的患者进行监测。如果受影响的TMJ植入物仍有库存且尚未进行植入操作,请联系Stryker公司。 2025年9月30日,Stryker公司向受影响的收货方发布了“紧急:医疗器械召回”通知。2025年12月4日和2026年2月25日,Stryker公司又向其他客户发布了延伸通知。这些通知建议采取以下措施:
(美国FDA网站)
|
|